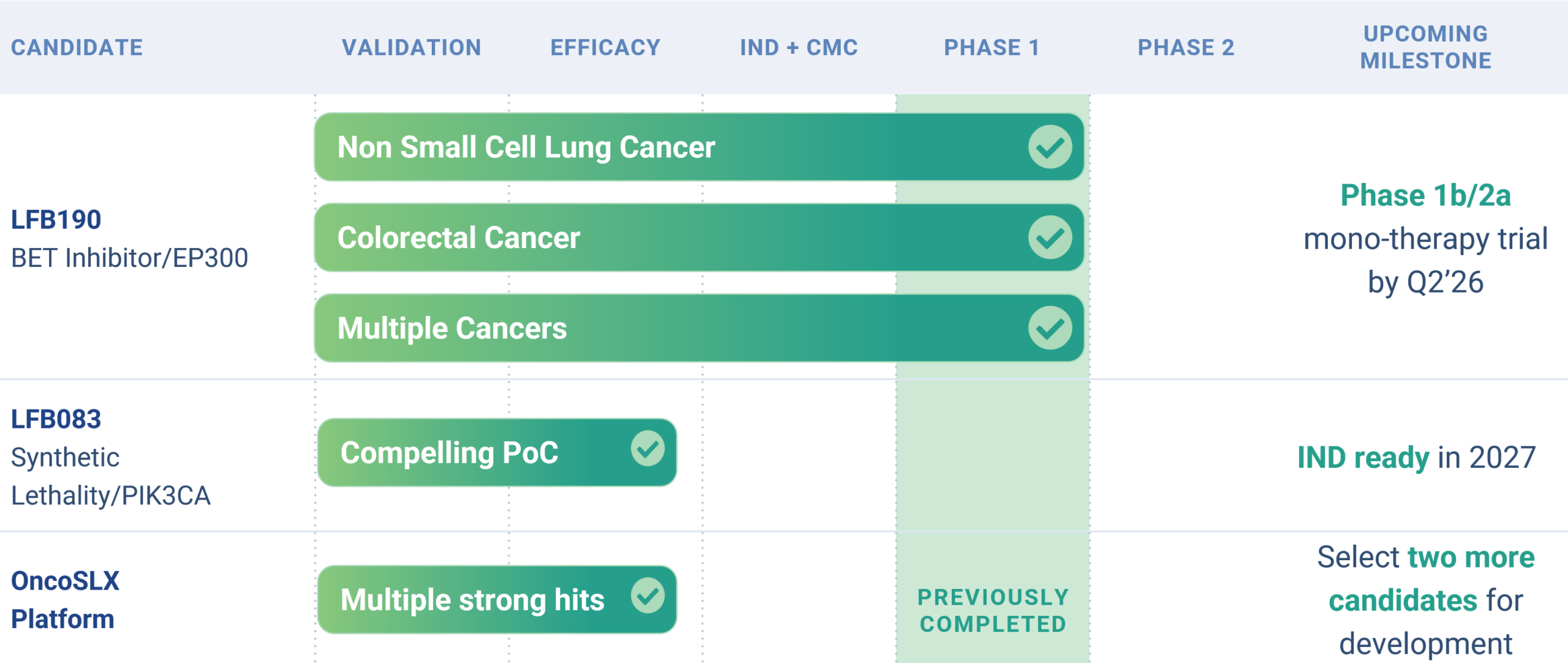
Pipeline
Candidats-médicaments
Le portefeuille de Leapfrog comprend plusieurs composés à petites molécules ayant déjà été évalués en contexte clinique et présentant un fort potentiel comme traitements majeurs pour des cancers définis sur le plan génétique. Les deux principaux programmes ont démontré un bon profil d’innocuité chez environ 100 patients non sélectionnés chacun.
LFB190
Parmi les centaines de criblages pharmacogénétiques que nous avons réalisés, l’effet de sensibilisation lié à la perte de fonction d’EP300 face à l’inhibition de BET se distingue par son ampleur et son importance, comparables à celles observées pour PARP dans les contextes BRCA1/HRD. Il figure parmi les résultats les plus marquants que nous ayons identifiés et se confirme dans tous les types de tumeurs où EP300 joue un rôle déterminant, ainsi qu’avec l’ensemble des inhibiteurs sélectifs de BET.
Leapfrog Bio prévoit lancer un essai clinique de phase 1b/2a en 2026 pour son principal programme, LFB190. LFB190 est un inhibiteur de BET de premier plan en développement pour le traitement des cancers porteurs de mutations avec perte de fonction (LOF) du gène EP300, une population de patients pour laquelle les besoins médicaux demeurent importants.
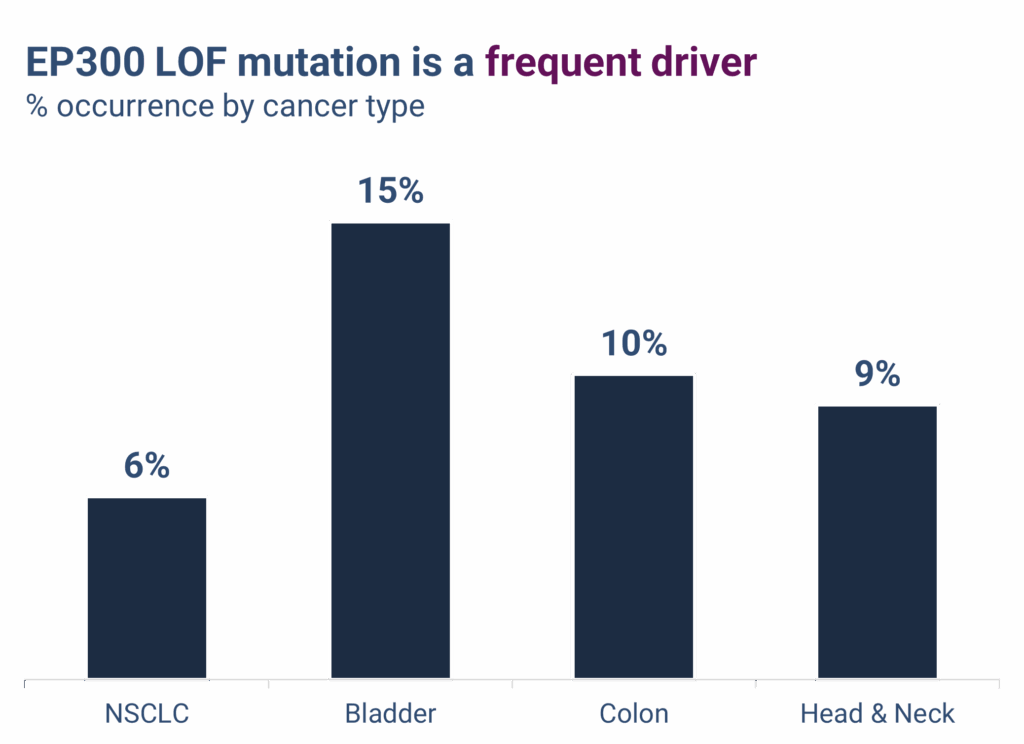
Les mutations avec perte de fonction (LOF) du gène EP300 sont des facteurs bien établis dans le développement de certains cancers et sont observées à des fréquences significatives dans plusieurs tumeurs solides, notamment :
- Cancer du poumon non à petites cellules (CPNPC) : ~6 %
- Cancer de la vessie : ~15 %
- Autres tumeurs solides majeures : 5 à 10 %, notamment les cancers de la tête et du cou, de l’œsophage, de l’estomac et de l’urothélium
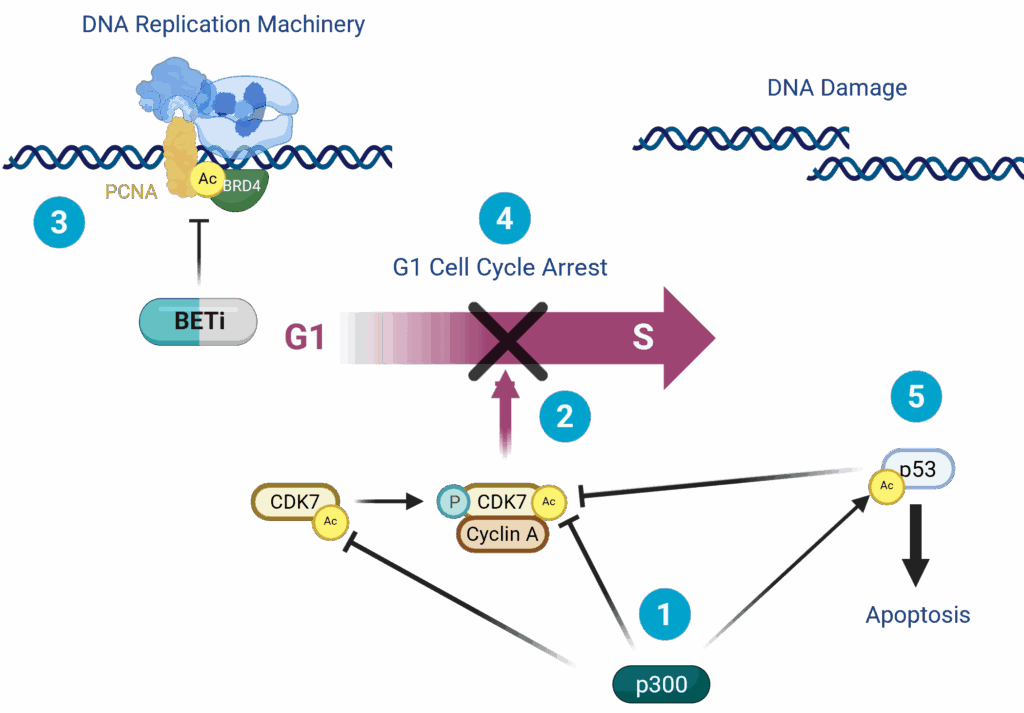
Nous et d’autres équipes avons montré que les inhibiteurs de BET (BETi) perturbent le recrutement de PCNA et de la machinerie de réplication de l’ADN dépendant de BRD4, ce qui entraîne généralement un arrêt du cycle cellulaire en phase G1. Toutefois, en présence de mutations avec perte de fonction (LOF) du gène EP300, la régulation des points de contrôle du cycle cellulaire lors de la transition G1-S est compromise, et les cellules poursuivent leur progression, ce qui entraîne une catastrophe mitotique et l’apoptose.
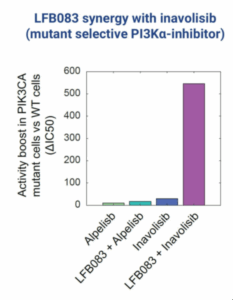

LFB083
Notre deuxième programme, LFB083, cible une interaction de létalité synthétique associée aux mutations avec gain de fonction du gène PIK3CA. Ces mutations sont à l’origine de plus de 100 000 cas de cancer par année aux États-Unis seulement, dont environ un tiers des cancers du sein. LFB083 augmente de plus de dix fois l’activité des inhibiteurs sélectifs de PI3K alpha ciblant les formes mutées, tout en ayant un impact minimal sur les cellules saines.