Recherche
S’attaquer aux mutations avec perte de fonction dans le cancer
Des progrès considérables ont été réalisés dans notre compréhension et le traitement du cancer. Différentes approches biologiques et thérapeutiques ont permis d’améliorer de façon significative les résultats cliniques. Certaines des avancées les plus marquantes reposent sur des thérapies ciblées conçues pour traiter des cancers associés à des mutations causales spécifiques dans des gènes clés, appelés gènes conducteurs.
Ces thérapies ont généralement été développées pour traiter des cancers associés à des mutations avec gain de fonction dans des gènes conducteurs, qui favorisent l’apparition et la progression de la maladie. Leur objectif est d’inhiber la fonction nouvellement acquise du gène ou les voies de signalisation qu’il active. Les gènes conducteurs présentant des mutations avec gain de fonction, aussi appelés oncogènes, sont responsables d’environ 30 % des cancers. La majorité des autres cancers sont plutôt liés à des mutations avec perte de fonction dans des gènes conducteurs qui, en temps normal, jouent un rôle de suppression tumorale. Ces gènes, appelés gènes suppresseurs de tumeurs, ne peuvent pas être ciblés directement lorsqu’ils sont mutés, puisque leur fonction est déjà inactive.
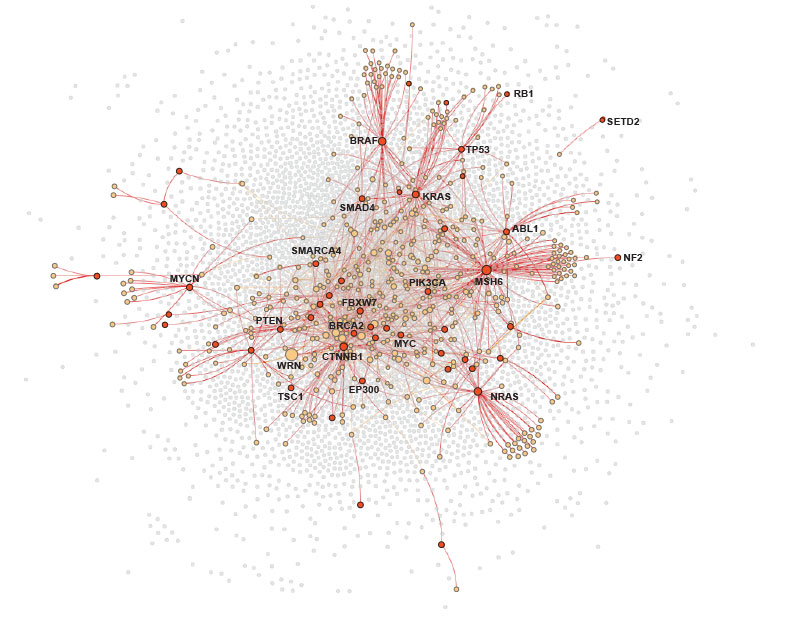
Accélérer les avancées en létalité synthétique
La létalité synthétique offre une voie prometteuse pour traiter les cancers associés à des mutations avec perte de fonction. Une relation de létalité synthétique se produit lorsque la perte de fonction simultanée de deux gènes entraîne la mort cellulaire, alors que la perte de fonction d’un seul de ces gènes n’a pas cet effet. Comme les cellules cancéreuses présentent déjà des altérations génétiques, une stratégie consiste à identifier puis à cibler pharmacologiquement un partenaire synthétiquement létal d’un de ces gènes. Les thérapies reposant sur cette approche, comme les inhibiteurs de PARP, permettent de traiter efficacement certains cancers tout en limitant les effets toxiques sur les cellules normales.
Réinventer les approches traditionnelles de létalité synthétique
Leapfrog redéfinit la façon dont les thérapies ciblées sur le plan génétique sont découvertes pour les cancers associés à des mutations avec perte de fonction. Les approches conventionnelles de létalité synthétique reposent sur des invalidations génétiques, à la fois pour reproduire la mutation causale et pour évaluer des cibles thérapeutiques potentielles. Or, les médicaments reproduisent rarement les effets d’une invalidation génétique et peuvent avoir des impacts cliniquement significatifs qui ne sont pas observés avec ce type d’approche. Notre plateforme OncoSLX surmonte ces limites grâce à une stratégie pharmacogénétique avancée et hautement optimisée, qui permet d’évaluer l’ensemble des effets biologiques des médicaments en synergie avec les mêmes perturbations causales qui sont à l’origine des tumeurs humaines.
Les médicaments font bien plus que simplement éliminer une protéine : ils peuvent bloquer des activités enzymatiques spécifiques, moduler des domaines fonctionnels distincts, modifier des états de modification post-traductionnelle propres à certains contextes cellulaires ou encore inhiber simultanément plusieurs protéines. Les inhibiteurs de PARP illustrent bien ce principe : leur forte synergie avec la perte de fonction de BRCA1 ne repose pas sur une simple reproduction d’une invalidation de PARP1, mais sur leur capacité à piéger PARP sur l’ADN — un mécanisme qui échappe aux approches classiques de létalité synthétique. En testant directement la biologie des médicaments en fonction des véritables mutations conductrices, OncoSLX permet de capter ces nuances pharmacologiques et de générer des résultats qui se traduisent en bénéfices pour les patients.
